SARS-CoV-2 Tempête de Cytokines (Cytokine Release Syndrom (CRS))
Dans la plupart des patients qui développent une COVID-19 sévère, les processus inflammatoires ne s'atténuent pas. Au lieu de cela, une tempête de cytokines émerge, une réponse hyper-inflammatoire impliquant l'activation dérégulée d'un grand nombre de cellules immunitaires et inflammatoires.
Les niveaux d'IL-6 continuent d'augmenter et les niveaux d'IL- 2, IL-7, IL-10, TNF-α, G-CSF, CXCL10, CCL2 et CCL3 sont également sensiblement plus élevés chez les patients sous COVID-19. Le nombre de lymphocytes T CD4+ et CD8+ est antiproportionnel aux niveaux de TNF-alpha, IL-6 et IL-10 chez les patients COVID-19. L'expression des marqueurs d'épuisement PD-1 et HAVCR2 est également augmentée dans ces cellules.D'autre part, dans les cas graves de COVID-19, le nombre de CD14+CD16+ monocytes inflammatoires est augmenté dans le sang périphérique. Les monocytes CD14+CD16+ ont également été liés à la maladie de Kawasaki, une maladie inflammatoire aiguë rare des artères chez les jeunes enfants qui a été observée récemment en conjonction avec COVID-19. Ces monocytes CD14+CD16+ sont aussi CD11b+ , CD14+ , CD16+ , CD68+ , CD80+ , CD163+ , CD206+ et sécrètent de l'IL-6, de l'IL-10 et du TNF-alpha, contribuant ainsi à l'inflammation.
Tous ces facteurs contribuent au développement d'un syndrome de libération de cytokines ou d'une tempête de cytokines, une réaction inflammatoire excessive dans laquelle des cytokines sont rapidement produites en grande quantité en réponse à une infection. La tempête de cytokines est considérée comme un facteur important du SDRA et du SDMO.
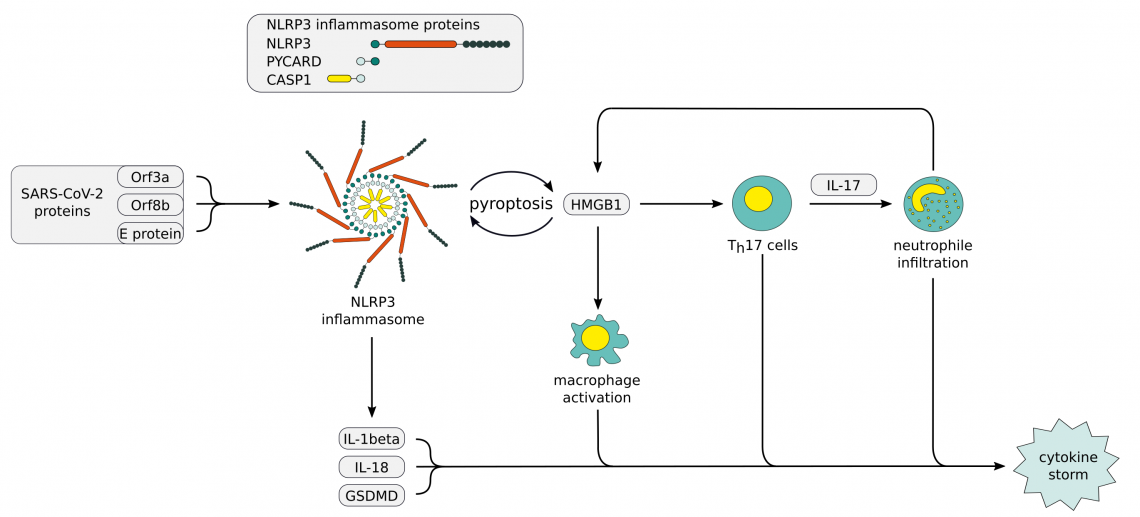
Des données suggèrent une susceptibilité accrue à une évolution grave de la COVID-19 en raison d'une inflammation de bas grade liée au mode de vie ou à la génétique. Ces facteurs peuvent conduire à une exposition accrue aux DAMP et à une activation supplémentaire de l'inflammasome NLRP3. L'un des DAMPs en aval de l'activation de l'inflammasome NLRP3 est le HMGB1. On le trouve généralement à des concentrations sériques élevées lors d'événements inflammatoires et agit comme médiateur central d'une réponse inflammatoire excessive en cas d'infections virales. Il a été proposé que l'HMGB1 soit l'un des principaux contributeurs à la tempête de cytokines par le biais d'une boucle de rétroaction positive impliquant l'induction de la production d'IL-17 par les cellules Th17 et l'infiltration subséquente de neutrophiles, conduisant à une nouvelle activation de l'inflammasome NLRP3.
La protéine SARS-CoV-2 N déclenche l'activation de la voie des lectines du système du complément par interaction avec la sérine-protéase associée à la lectine liant le mannose (MBL) (MASP)2. Les dimères solubles de la protéine N libérés interagissent avec la MASP-2, accélérant encore l'activation de la MASP-2 et l'activation du système du complément. La rétroaction positive par la lyse cellulaire et la libération de la protéine N entraîne une augmentation supplémentaire des cytokines pro-inflammatoires et une aggravation de la tempête de cytokines.
En plus de l'effet dommageable sur la structure alvéolaire, les cytokines inflammatoires IL-1 et TNF induisent une augmentation de l'expression de la HA-synthase-2 (HAS2) dans l'endothélium CD31+, les cellules épithéliales alvéolaires EpCAM+ du poumon et les fibroblastes. Le HAS2 catalyse la polymérisation de l'hyaluronane, un composant de la matrice extracellulaire qui peut absorber de l'eau jusqu'à 1000 fois son poids. L'accumulation de cette gelée liquide dans les poumons endommagés limite encore plus l'échange gazeux dans le poumon, ce qui entraîne une faible saturation du sang en oxygène.

Gratuit: Manuel sur le SRAS-CoV-2
49 pages * Téléchargement gratuit * Anticorps et protéines * Lignées du SRAS-CoV-2 * Mutations et implications pour les NAbs
Plus d'informations et téléchargementAnticorps liés à la tempête de cytokines:
- (1)
- (7)
- (2)
- (7)
- (2)
- (6)
- (2)
- (5)
- (8)
- (5)
- (8)
- (3)
- (2)
- (1)
- (2)
- (1)
- (2)
- (1)
- (2)
Kits ELISA liés à la tempête cytokine:
(Pre-coated)
- (55)
- (6)
(Pre-coated)
- (25)
- (6)
(Pre-coated)
- (31)
- (5)
(Pre-coated)
- (16)
- (5)
(Pre-coated)
- (4)
- (5)
(Pre-coated)
- (8)
- (5)
(Pre-coated)
- (4)
- (5)
(Pre-coated)
- (4)
- (4)
Information et produits connexes
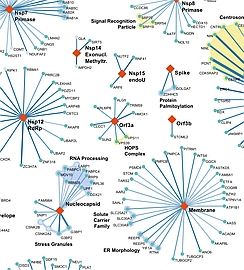
SARS-CoV Protein Interactome / poster and products
NLRP3 inflammasome, poster and products
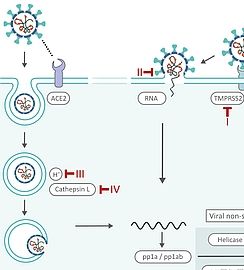
SARS-CoV-2 Life Cycle: Stages and Inhibition Targets
Références
: "Imbalanced Host Response to SARS-CoV-2 Drives Development of COVID-19." dans: Cell, Vol. 181, Issue 5, pp. 1036-1045.e9, (2020) (PubMed).: "ORF8 contributes to cytokine storm during SARS-CoV-2 infection by activating IL-17 pathway." dans: iScience, Vol. 24, Issue 4, pp. 102293, (2021) (PubMed).
: "The trinity of COVID-19: immunity, inflammation and intervention." dans: Nature reviews. Immunology, Vol. 20, Issue 6, pp. 363-374, (2020) (PubMed).
: "Severe COVID-19: NLRP3 Inflammasome Dysregulated." dans: Frontiers in immunology, Vol. 11, pp. 1580, (2020) (PubMed).
: "The CD14+ CD16+ blood monocytes: their role in infection and inflammation." dans: Journal of leukocyte biology, Vol. 81, Issue 3, pp. 584-92, (2007) (PubMed).
- Gao, T. et al. Highly pathogenic coronavirus N protein aggravates lung injury by MASP-2- mediated complement over-activation. medRxiv (2020). doi:10.1101/2020.03.29.20041962
- Fan, X. et al. Changes of Damage Associated Molecular Patterns in COVID-19 Patients. Infectious Diseaeses & Immunity (2021). doi:10.1097/01.id9.0000733572.40970.6c
- Zhang, D. et al. COVID-19 infection induces readily detectable morphological and inflammation-related phenotypic changes in peripheral blood monocytes, the severity of which correlate with patient outcome. medRxiv (2020). doi:10.1101/2020.03.24.20042655