CUT&Tag
CUT&Tag (Cleavage Under Targets and Tagmentation) offre une nouvelle approche pour poursuivre l'épigénétique. La méthode est conçue pour cartographier les variantes d'histones et les modifications post-traductionnelles à l'échelle du génome, les sites de liaison des facteurs de transcription et les complexes associés à la chromatine.
CUT&Tag Workflow

CUT&Tag est réalisé in situ sur des cellules immobilisées et intactes sans réticulation. La fragmentation de l'ADN est obtenue par le marquage de l'ADN génomique par une transposase Tn5 hyperactive qui est chargée de duplex adaptateurs de séquençage et fusionnée à la protéine A et/ou à la protéine G (pA/G-Tn5). La protéine de fusion est liée, via ses fragments de protéine A et/ou de protéine G, à un anticorps dirigé contre la cible souhaitée, ce qui entraîne un marquage à proximité de l'antigène ciblé. Les produits CUT&Tag conviennent à la génération de bibliothèques pour le séquençage de nouvelle génération (NGS) sans autre étape de polissage final.
Avantages du CUT&Tag
- Performé in situ sur des cellules non fixées ; aucune fragmentation de la chromatine n'est nécessaire.
- Faible bruit de fond et haute sensibilité nécessitent une faible profondeur de séquençage.
- Aucune étape de polissage des extrémités et de ligature des adaptateurs de séquençage n'est nécessaire.
- Possible avec de faibles nombres de cellules jusqu'à 100 cellules selon l'antigène.
- Simple, rapide, se prêtant à l'automatisation.
- Quantification précise en utilisant le carry-over E. coli ADN de la purification pAG-Tn5.
Manuel CUT&RUN + CUT&Tag
Obtenez votre exemplaire gratuit de notre tout nouveau manuel pour CUT&RUN et CUT&Tag!
Produits pour le CUT&Tag
antibodies-online propose des solutions flexibles pour vos expériences CUT&Tag. Choisissez vous-même des anticorps de contrôle, des anticorps secondaires ou des billes magnétiques parmi notre offre de produits CUT&Tag ; contactez notre équipe de biologistes pour obtenir un ensemble de réactifs finement réglés, ainsi qu'un protocole optimisé.
- CUT&Tag Anticorps secondaire
- Amplification du signal dans CUT&Tag
- Fixation efficace de la fusion pAG-Tn5
- Convient aux essais CUT&Tag
- Manipulation supérieure à celle des billes de silice ConA, performances comparables.
- Validé pour CUT&RUN et CUT&Tag
- Détecte spécifiquement les IgG de souris (H&L)
- 3 Citations PubMed disponibles
Anticorps épigénétiques pour CUT&Tag
antibodies-online propose des anticorps contre des modifications d'histones et des facteurs de transcription abondants. Ils conviennent en tant que contrôle positif et sont importants pour évaluer le succès de la méthode CUT&Tag.
Questions fréquemment posées
Comment choisir entre CUT&RUN et CUT&Tag ?
Dans la méthode CUT&Tag, les amorces de séquençage sont fixées à l'ADN clivé et aucune étape supplémentaire d'annexion n'est nécessaire. Cette méthode fonctionne bien pour les protéines nucléosomiques et les protéines étroitement liées. Cette méthode est également moins susceptible de produire un signal de fond dû à des dommages à l'ADN.
CUT&RUN en revanche est préférable pour les facteurs de transcription (complexes) ou les protéines moins étroitement liées à l'ADN. Il a également une meilleure résolution que CUT&Tag.
Est-il possible d'utiliser CUT&Tag avec des échantillons de tissus végétaux ?
CUT&Tag sur des cellules végétales isolées a été décrit pour le profilage des marques d'histones H3K4me3 dans différents types de tissus de coton en utilisant des noyaux isolés14. Nos anticorps H3K27me3 H3K4me3 de contrôle positif et l'anticorps IgG anti-lapin de cobaye de contrôle négatif ainsi que les billes de ConA sont adaptés à une utilisation avec des échantillons de plantes.
Puis-je dénaturer les protéines du complexe de produits CUT&Tag au lieu d'un traitement à la protéinase K ?
Nous déconseillons cette option : l'ADN d'intérêt est à son moment présent dans un complexe constitué de l'ADN, de la protéine d'intérêt, de l'anticorps correspondant et du pA/G-Tn5. L'ébullition de ce complexe précipitera probablement l'ADN avec la protéine dénaturée. Cela affectera aussi principalement les produits CUT&Tag courts et non les molécules d'ADN plus grandes, ce qui entraînera une diminution du rapport signal/bruit dans votre bibliothèque et réduira potentiellement aussi la complexité de la bibliothèque. Cet effet est encore exacerbé en raison de la température de fusion plus basse de ces molécules courtes par rapport aux molécules d'ADN contaminantes plus longues.
Quels anticorps secondaires puis-je utiliser pour CUT&Tag?
- (105)
- (3)
- (2)
- (4)
- (1)
Puis-je utiliser les billes AMPure CP pour purifier les produits de tagmentation au lieu de l'extraction phénol-chloroforme ?
Dans la publication originale décrivant la méthode CUT&Tag, les auteurs mentionnent l'utilisation de billes AMPure XP pour la purification de l'ADN après marquage et digestion à la protéinase K1. Un problème potentiel est le transfert de la protéinase K active, qui peut interférer avec l'amplification PCR en aval. Par conséquent, les auteurs recommandent maintenant l'extraction phénol-chloroforme pour assurer la dénaturation complète de la protéinase K15.
Pourquoi le rendement en ADN est-il si faible ?
La méthode CUT&Tag est réalisée en utilisant un faible nombre de cellules et le signal de fond est considérablement plus faible que par exemple pour le ChIP. En raison de ces deux facteurs, la quantité d'ADN récupérée est souvent trop faible pour être mesurée de manière fiable sur la base d'un dosage fluorométrique ou par électrophorèse capillaire. L'amplification par PCR de petits produits CUT&RUN, c'est-à-dire inférieurs à 50 pb, peut être problématique et n'est donc pas une option.
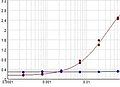
Afin d'évaluer le succès de la méthode CUT&Tag, incluez un ou plusieurs échantillons témoins positifs en utilisant l'anticorps témoin positif H3K4m3 ABIN3023254 et/ou l'anticorps témoin positif H3K27me3 ABIN6923144. Les fragments d'ADN préparés à l'aide de ces anticorps peuvent être mesurés par électrophorèse sensible sur un Bioanalyzer ou Tapestation ou par fluorométrie sur un fluoromètre Qubit ou Nanodrop. Lorsque l'on utilise le contrôle positif CUT&RUN ABIN6923144 (point rouge) (ou tout autre anticorps spécifique des marqueurs nucléosomiques), une échelle correspondant à des multiples des nucléosomes de 147 pb de long devrait être visible par électrophorèse capillaire.
Informations et produits connexes
CUT&RUN - clivage sous cibles et libération par nucléase : Informations et produits
References
: "Efficient chromatin profiling of H3K4me3 modification in cotton using CUT&Tag." dans: Plant methods, Vol. 16, pp. 120, (2020) (PubMed).: "Improved CUT&RUN chromatin profiling tools." dans: eLife, Vol. 8, (2019) (PubMed).
: "The three-dimensional structure of a Tn5 transposase-related protein determined to 2.9-A resolution." dans: The Journal of biological chemistry, Vol. 274, Issue 17, pp. 11904-13, (1999) (PubMed).
: "ChIC and ChEC; genomic mapping of chromatin proteins." dans: Molecular cell, Vol. 16, Issue 1, pp. 147-57, (2004) (PubMed).
: "Multiplex single cell profiling of chromatin accessibility by combinatorial cellular indexing." dans: Science (New York, N.Y.), Vol. 348, Issue 6237, pp. 910-4, (2015) (PubMed).
: "An efficient targeted nuclease strategy for high-resolution mapping of DNA binding sites." dans: eLife, Vol. 6, (2018) (PubMed).
: "CUT&Tag for efficient epigenomic profiling of small samples and single cells." dans: Nature communications, Vol. 10, Issue 1, pp. 1930, (2019) (PubMed).
Henikoff, S. & Henikoff, J. G. Profiling the epigenome at home. bioRxiv 1–18 (2020). doi:10.1101/2020.04.15.043083
Bartosovic, M., Kabbe, M. & Castelo-Branco, G. Single-cell profiling of histone modifications in the mouse brain. bioRxiv 2020.09.02.279703 (2020). doi:10.1101/2020.09.02.279703
Wu, S. J. et al. Single-cell analysis of chromatin silencing programs in developmental and tumor progression. bioRxiv 2020.09.04.282418 (2020). doi:10.1101/2020.09.04.282418
Kaya-Okur, H., Henikoff, S. & Henikoff, S. Bench top CUT&Tag. protocols.io 1–19 (2019). Available at: https://www.protocols.io/view/bench-top-cut-amp-tag-z6hf9b6.




